

Задачи № 2, 5, 9
s003.radikal.ru/i202/1009/0a/ffb385eaefe8.jpg
Заранее спасибо!))
задача легкая, но я за лето все забыла. если составите хотя бы уравнение реакций, буду премного благодарна.
ПОМОГИТЕ ПОЖАЛУЙСТА!!
работу должна сдать 9 сентября...

помогите,пожалуйста!! может кто-нибудь ОЧЕНЬ подробно расписать,как определяется валентность по таблице Менделеева? проблема у доброй части восьмого класса (не подумайте,что мы идиоты - учитель невразумительный достался). знаем,что есть постоянная валентность элементов - ладно. что делать с непостоянной?
1.Рассчитайте молярную концентрацию эквивалента Сf кислот:
если в 300 мл расствора соляной кислоты содержиться 18.25 г хлороводорода
Заранее огромное спасибо!!!
Всем привет, простите за вторжение)
Продаю следующий книги по заниженой цене (пожелали некоторое время на полке, чистенькие и не использованые):
Физика. Кабардин. Справочник для старшеклассников и поступающих в вузы: полный курс подготовки к выпускным и вступительным экзаменам. 70 рэ
ЕГЭ История. Универсальный справочник.2010 70 рэ
ЕГЭ математика. Типовые тестовые задания. 2010. 20 рэ
Тригонометрия. 10 класс («просвещение») – тут формулы по темам, задачи, решения к ним. 20 рэ
ЕГЭ Литература тренировочные задания 2009 40 рэСборник задач по физике 7-9 класс Лукашик, Иванова 50 рэ
Физика Задачник 10-11 класс Рымкевич 50 рэ
Краткий курс школьной математики Битнер – формулы, теоремы, задачи с решениями, просто задания 100 рэ
Решебник задач по физике в помощь поступающим в вузы Фомина – задачи с объяснением решений 100 рэ
Произведения школьной программы 11 класса краткое изложение «Астрель» Родин, Пименова 70 рэ
Сборник задач по математике (геометрия) поступающим в вузы под редакцией Сканави (с решениями) 70 рэ
ЕГЭ история 2010 сборник экзаменационных заданий 40 рэ
ЕГЭ обществознание сборник заданий 2010-07-17 40 рэ
ЕГЭ литература сборник экзаменационных заданий 2010 40 рэ
История России в таблицах и схемах часть 2 Ивашко (17 – первая половина 18 века) 30 рэ
Литература для выпускников и абитуриентов (анализ произведений) 2009 «Эксмо» Амелина 70 рэ
Логика учебное пособие 10-11 класс «Кнорус» 70 рэ
L`oiseau Bleu (синяя птица) сборник упражнений 7-8 класс (французский) 50 рэ
Домашняя работа по химии 11 класс (Габриелян, Лысова) 30 рэ
Домашняя работа по алгебре 10 класс (Мордкович) 30 рэ
Домашняя работа по геометрии 10 класс (Атанасян, Бутузов, Кадомцев) 30 рэ
Математика самостоятельные и контрольные работы 6 класс (Ершова) 30 рэ
Алгебра Геометрия самостоятельные и контрольные работы 7 класс (Ершова) 30 рэ
Алгебра Геометрия самостоятельные и контрольные работы 8 класс (Ершова) 30 рэ
Алгебра Геометрия самостоятельные и контрольные работы 9 класс (Ершова) 30 рэ
Алгебра и начала анализа 10-11 класс самостоятельные и контрольные работы (Ершова) 30 рэ
Конституция Российской Федерации с комментариями для изучения и понимания 30 рэ
Алгебра и начала анализа самостоятельные работы 10 класс (Александрова)
Пишите на умыл, могу кинуть фото книги)))
а) Соль - Na2S
Молярная концентрация соли, С(x), моль/дм3 - 0,1
Константа диссоциации слабой кислоты или основания, Кд - КдI (H2S) = 1,05 · 10-7
б) Соль - Al2(SO4)3
Молярная концентрация соли, С(x), моль/дм3 - 0,1
Константа диссоциации слабой кислоты или основания, Кд - КдIII (Al(OH)3) = 1,38 · 10-9
2) Напишите формулу мицеллы золя, полученного сливанием 60 см3 раствора нитрата серебра AgNO3 с молярной концентрацией 0,05 моль/дм3 и 30 см3 раствора иодида калия Kl с молярной концентрацией 0,01 моль/дм3.
3) Золь иодида серебра был получен при добавлении избытка Kl к раствору AgNO3. Определите заряд частиц полученного золя и напишите формулу его мицеллы.
4) Вода, содержащая только сульфат магния, имеет жесткость
7 ммоль/л. Какая масса сульфата магния содержится в 300 л этой воды?
5) Какие ионы надо удалить из природной воды, чтобы сделать ее мягкой? Введением каких ионов можно умягчить воду? Составьте уравнения соответствующих реакций. Какую массу Ca(OH)2 надо прибавить к 2,5 л воды, чтобы устранить ее жесткость, равную 4,473 ммоль/л.
Решите кто сколько сможет, и желательно расписать как, в тетради надо будет писать, если не сложно...заранее спасибо...
никак не могу понять механизм реакции гидролиза жира примерно такого типа:
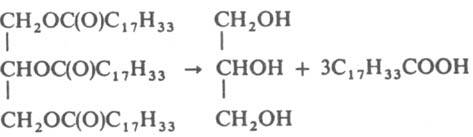
что к чему будет присоедиться? какого типа реакция? нуклеофильное замещение?

читать дальше
и еще не понимаю, что такое 0,1
буду очень благодарна хоть какой-нибудь помощи
2. При нагревании 10 л воды образовался осадок карбоната кальция массой 2,5 г. Чему была равна величина временной жесткости воды?
3. Приведите формулы двух веществ, в одном из которых селен может быть только восстановителем, а в другом — только окислителем.
4. Уравняйте реакции, укажите окислитель и восстановитель:
Na2S+K2Cr2O7 + H2SO4 → S + Cr2(SO4)3 + Na2SO4 + K2SO4 + H2O
CuI2 → CuI + I2
5. Закончить уравнения реакций:
Zn + HNO3 (разб.) →
Cu + H2SO4 (конц.) →
6. На сплав Al и Cu массой 10 г подействовали избытком концентрированно-го раствора NaOH. Выделилось 3,36 л газа (при н.у.). Вычислите процент-ный состав сплава
Вариант 2
1. Как зависит скорость коррозии железа и цинка от рН среды?
2. Двойной электрический слой на границе металл─раствор его соли. Элек-тродный потенциал. Стандартный водородный электрод.
3. Свойства эстрих-гипса, его отличия от строительного. Рассчитать расход кокса для получения 100 т эстрих-гипса (содержание СаО принять равным 10 %), если учесть, что производство эстрих-гипса основано на реакции:
CaSO4 + C → CaO + SO2 + CO
4. Глиноземнистый цемент. Получение. Особенности гидратации. Привести уравнения соответствующих реакций.
5. Сколько граммов брома могут присоединить 5 л смеси, состоящей из 32,8 % метана, 22,4 % ацетилена и 44,8 % этилена (по объему)? Напишите реакцию ступенчатой полимеризации (поликонденсации) фенола с избыт-ком формальдегида в щелочной среде. Отношение полученного полимера к нагреванию. Область применения.
Заранее Спасибо
Итак, тут представлены чудеснейшие задачки по химии из программы 1 курса, предмет ксе. Уровень задачек 11-10класс. Под морем - пир для ума!
чудеса науки
CvH2= 18.97 + 3.26*10-3 T + 0.502*105 T-2 Дж/(моль*К)
(то же самое для О2 и H2O)
Удельная теплота сгорания водорода с образованием жидкой воды при 0 градусов равна -142,2 кДж/Г. Удельная теплота испарения воды при 0 градусов равна 2551 Дж/г.
Рассчитать молярную теплоту образования водяного пара.
Мое решение
У какого элемента потенциал ионизации выше?
Ртуть
Германий
Селен
Кадмий
Иттрий
Сродство к электрону ниже у элемента
Углерод
Сера
Кремний
Азот
Бром
Помоги с решением, задача вроде простая, но не могу сделать.
Будет ли какое-то уравнение реакции? А оно должно быть, ибо мне нужно найти изменение энтропии.
Какая масса воды образуется при сгорании в кислороде 5 парафиновых свечей массой 100 г каждая, если массовая доля углерода в этом образце парафина составляет 80%?
2.
Какая масса сажи образуется при термическом разложении этана массой 90 г? Массовая доля выхода сажи составляет 80%.
3.
Какой объем водорода можно получить из 20 м3 природного газа, содержащего 93% метана, 4% этана и 3% азота и углекислого газа? Кроме водорода в процессе пиролиза образуется сажа.
4.
При нитровании 4,48 л этана (н.у.) азотной кислотой получили 12 г нитроэтана C2H5NO2. Вычислите массовую долю выхода продукта.
Уровень - 1-й курс педагогического ВУЗа, естественно-географический факультет, кафедра биологии. Контрольная. Крайний срок - 7:00 15-го июня (вторник). Буду очень благодарна, если кто-то откликнется!
Задачи
1. Вычислить pH и степень гидролиза соли в 0,05М Na2CO3. Чем будет равен pH, если раствор разбавить водой в 5 раз?
2. Вычислить pH раствора, полученного смешением 210 мл 0,1М Na2CO3 и 90 мл 0,1М HCl
3. Определить концентрацию раствора уксусной кислоты, если α=2%, Ka=1,75х10-5
4. В 0,5 л соляной кислоты содержится 0,1 моль HCl. Определить массовую долю кислоты в растворе.





















